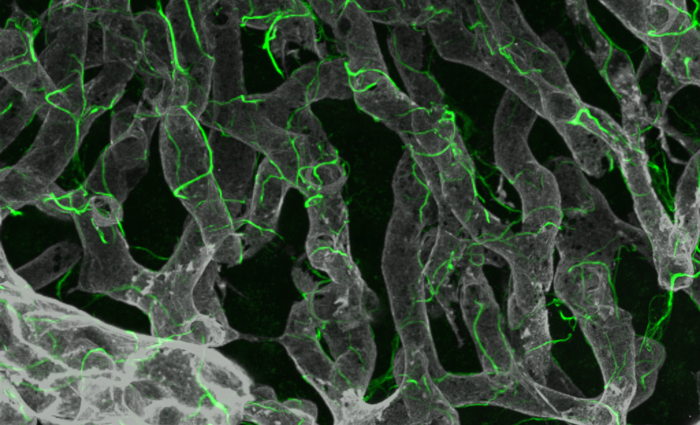
Uno studio su topi e cellule umane suggerisce che un farmaco antitumorale esistente può essere efficace contro la malattia.
Utilizzando le ultime tecnologie, tra cui sia il sequenziamento nucleare singolo di topi e tessuto epatico umano, sia l’imaging avanzato in vetro 3D nei topi per caratterizzare le cellule epatiche produttrici di cicatrici chiave, i ricercatori hanno scoperto nuovi bersagli farmacologici candidati per la steatosi epatica non alcolica (NAFLD). La ricerca è stata condotta da ricercatori della Icahn School of Medicine del Monte Sinai.
Utilizzando questi metodi innovativi, i ricercatori hanno scoperto una rete di comunicazione cellula-cellula che guida le cicatrici man mano che la malattia epatica avanza. I risultati, pubblicati online il 4 gennaio su Science Translational Medicine, potrebbero portare a nuovi trattamenti.
Caratterizzata da grasso nel fegato e spesso associata a diabete di tipo 2, ipertensione e lipidi nel sangue elevati, la NAFLD è una minaccia mondiale. Negli Stati Uniti, si stima che il 30-40% degli adulti sia affetto, con circa il 20% di questi pazienti che hanno uno stadio più avanzato chiamato steatoepatite non alcolica, o NASH, che è caratterizzato da infiammazione del fegato e può progredire verso cicatrici avanzate (cirrosi) e insufficienza epatica.
La NASH è anche la causa di cancro al fegato in più rapida crescita in tutto il mondo. Poiché gli stadi avanzati della NASH sono causati dall’accumulo di fibrosi o cicatrici, i tentativi di bloccare la fibrosi sono al centro degli sforzi per trattare la NASH, ma nessun farmaco è attualmente approvato per questo scopo, affermano i ricercatori.
Come parte degli esperimenti, i ricercatori hanno eseguito il sequenziamento nucleare singolo in studi paralleli su entrambi i modelli murini di NASH e tessuto epatico umano da nove soggetti con NASH e due controlli.
Hanno identificato un numero condiviso di 68 coppie di potenziali bersagli farmacologici tra le due specie. Inoltre, i ricercatori hanno perseguito una di queste coppie testando un farmaco antitumorale esistente nei topi.
“Abbiamo mirato a comprendere la base di questa cicatrizzazione fibrotica e identificare bersagli farmacologici che potrebbero portare a nuovi trattamenti per la NASH avanzata studiando le cellule stellate epatiche, che sono le cellule chiave che producono cicatrici nel fegato”, ha detto l’autore senior dello studio Scott L. Friedman, Irene e Dr. Arthur M. Fishberg Professor of Medicine, Dean for Therapeutic Discovery, e capo delle malattie del fegato a Icahn Mount Sinai.
“Combinando questo nuovo approccio di imaging del fegato insieme all’analisi dell’espressione genica nelle singole cellule, abbiamo svelato una comprensione completamente nuova di come queste cellule generano cicatrici mentre la NASH avanza verso le fasi avanzate”.
I ricercatori hanno scoperto che nella malattia avanzata, le cellule stellate sviluppano una fitta rete, o meshwork, di interazioni tra loro che facilitano queste 68 coppie di interazione uniche non precedentemente identificate in questa malattia.
“Abbiamo confermato l’importanza di una di queste coppie di proteine, NTF3-NTRK3, utilizzando una molecola già sviluppata per bloccare NTRK3 nei tumori umani e l’abbiamo riproposta per stabilire il suo potenziale come nuovo farmaco per combattere la fibrosi NASH”, ha detto il primo autore Shuang (Sammi) Wang.
“Questa nuova comprensione dello sviluppo della fibrosi suggerisce che la fibrosi avanzata può avere un repertorio unico di segnali che accelerano le cicatrici, che rappresentano un insieme precedentemente non riconosciuto di bersagli farmacologici”.
I ricercatori ipotizzano che i circuiti di come le cellule comunicano tra loro si evolvono man mano che la malattia progredisce, quindi alcuni farmaci possono essere più efficaci prima e altri in fasi più avanzate. E lo stesso farmaco potrebbe non funzionare per tutte le fasi della malattia.
I ricercatori stanno attualmente lavorando con i chimici di Icahn Mount Sinai per ottimizzare ulteriormente gli inibitori NTRK3 per il trattamento della fibrosi epatica.
Successivamente, i ricercatori hanno in programma di esaminare funzionalmente tutti gli interattori candidati in un sistema di coltura cellulare, seguito da test in modelli preclinici di malattia epatica, come hanno fatto per NTRK3.
Inoltre, sperano di estendere i loro sforzi per determinare se interazioni simili tra le cellule fibrogeniche sono alla base della fibrosi di altri tessuti tra cui cuore, polmone e reni.
Immadine: Wang, et al., Sci. Transl. Med. [volume 15], [add3949] [(2023)]