I dati a 48 settimane dello studio clinico di fase III MOMENTUM dimostrano che momelotinib ha mantenuto la risposta totale ai sintomi, l’indipendenza trasfusionale e la risposta splenica nella maggior parte dei pazienti che hanno risposto al trattamento.
I nuovi dati a 48 settimane dello studio di fase III MOMENTUM hanno mostrato come dopo essere stati sottoposti a momelotinib, la maggior parte dei pazienti affetti da mielofibrosi, precedentemente trattati con un inibitore della Janus chinasi (JAK), ha mantenuto le proprie risposte misurate secondo specifici parametri clinici, tra cui il punteggio totale dei sintomi (TSS), l’indipendenza trasfusionale ( TI) e il tasso di risposta splenica (SRR).
Inoltre, nuove analisi di MOMENTUM hanno evidenziato che la risposta TI con momelotinib alla 24esima settimana era associata alla sopravvivenza globale. Questi dati sono stati presentati al 64° meeting annuale dell’American Society of Hematology (ASH) (10-13 dicembre) in corso a New Orleans.
Hesham Abdullah, Senior Vice President, Global Head of Oncology Development, GSK, ha commentato: “I pazienti con mielofibrosi hanno bisogni medici significativi, inclusa l’anemia progressiva derivante dalla malattia e spesso esacerbata dai trattamenti attualmente a disposizione. I dati presentati oggi rafforzano il potenziale di momelotinib come opzione terapeutica con un impatto favorevole sui sintomi della mielofibrosi e sul volume della milza, nonché sulle trasfusioni di sangue dovute all’anemia”.
MOMENTUM è uno studio clinico globale, randomizzato, in doppio cieco di fase III che confronta momelotinib (MMB) con danazolo (DAN) in pazienti con mielofibrosi sintomatici e anemici precedentemente trattati con un inibitore JAK approvato.
Lo studio è stato progettato per valutare la sicurezza e l’efficacia di momelotinib per il trattamento e la riduzione delle principali manifestazioni della malattia: sintomi costituzionali, trasfusioni di sangue (dovute ad anemia) e ingrossamento della milza.
I pazienti sono stati randomizzati in rapporto 2:1 per ricevere momelotinib o danazolo (n=130 e n=65, rispettivamente). Dopo 24 settimane di trattamento, ai pazienti trattati con danazolo è stato permesso di passare al trattamento con momelotinib.
Il crossover precoce a momelotinib è stato suggerito dalla progressione splenica confermata. L’analisi primaria alla settimana 24 ha raggiunto l’endpoint primario di riduzione del TSS di ≥50% nei 28 giorni immediatamente prima della fine della settimana 24 rispetto al TSS al basale, utilizzando il modulo di valutazione dei sintomi della mielofibrosi.
Ha inoltre soddisfatto gli endpoint secondari chiave, tra cui il tasso di TI per ≥12 settimane immediatamente prima della fine della settimana 24 con livelli di emoglobina ≥ 8 g/dL e SRR basato su una riduzione del volume splenico di ≥35% alla settimana 24 rispetto al basale.
I dati di follow-up a 48 settimane da MOMENTUM presentati all’ASH hanno dimostrato quanto segue (presentazione orale n. 627):
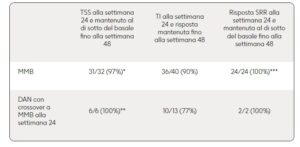
*12 dei 61 (20%) pazienti non responsivi che hanno ricevuto momelotinib alla settimana 24 hanno raggiunto una risposta TSS alla settimana 48
**10 dei 35 (29%) pazienti non rispondenti che hanno ricevuto danazolo e sono passati a momelotinib alla settimana 24 hanno ottenuto una nuova risposta TSS alla settimana 48
Dati disponibili per 24 dei 30 pazienti che hanno ricevuto momelotinib e hanno raggiunto la risposta splenica a 24 settimane
Nello studio MOMENTUM, gli eventi avversi emergenti dal trattamento di grado 3 o superiore più comuni nel periodo in aperto, simili al periodo in doppio cieco, sono stati trombocitopenia (9% per il braccio di trattamento continuo con momelotinib e 15% per il braccio di trattamento da danazolo a momelotinib) e anemia (9% per il braccio di trattamento continuo con momelotinib e 2% per il braccio di trattamento da danazolo a momelotinib). Inoltre, questi risultati di efficacia e sicurezza nei pazienti con trombocitopenia sono stati coerenti con la popolazione complessiva.
Un’ulteriore analisi dello studio clinico MOMENTUM ha valutato l’impatto della risposta TI sulla sopravvivenza globale (abstract #3028). Come presentato in precedenza, i pazienti trattati con momelotinib avevano maggiori probabilità di raggiungere l’indipendenza trasfusionale durante il periodo di studio rispetto ai pazienti trattati con danazolo.
I pazienti trattati con momelotinib avevano anche meno probabilità di richiedere una trasfusione durante il periodo di studio (il 35% dei pazienti trattati con momelotinib aveva zero unità trasfuse rispetto al 17% dei pazienti con danazolo) e più probabilità di ridurre il carico trasfusionale.
I dati presentati all’ASH con follow-up di sopravvivenza aggiuntivo suggeriscono che la risposta TI con momelotinib alla settimana 24 è associata alla sopravvivenza globale rispetto ai pazienti che non erano TI.
Una domanda di nuovo farmaco e una domanda di autorizzazione all’immissione in commercio per momelotinib sono attualmente in fase di revisione rispettivamente con la Food and Drug Administration (FDA) statunitense e l’Agenzia europea per i medicinali (EMA). Momelotinib non è attualmente approvato in nessun mercato.
Momelotinib è un trattamento orale sperimentale per la mielofibrosi. Momelotinib non solo inibisce la via di segnalazione della Janus chinasi (JAK) 1 e le vie di segnalazione JAK2, ma anche il recettore dell’activina A di tipo I (ACVR1). L’inibizione di JAK1 e JAK2 può migliorare i sintomi costituzionali e la splenomegalia.
Inoltre, l’inibizione diretta di ACVR1 porta ad una diminuzione dell’epcidina circolante, che è spesso elevata nella mielofibrosi e contribuisce all’anemia.
La mielofibrosi è un tumore raro e potenzialmente fatale caratterizzato dall’accumulo di tessuto cicatriziale eccessivo nel midollo osseo, che interferisce con la produzione di cellule del sangue sane e può portare a: grave basso numero di sangue, tra cui anemia e trombocitopenia; sintomi costituzionali come debolezza e affaticamento; e splenomegalia o un ingrossamento della milza.
La mielofibrosi colpisce circa 1 persona su 500.000 in tutto il mondo. Al momento della diagnosi, circa il 40% dei pazienti è anemico e quasi tutti i pazienti affetti da mielofibrosi svilupperanno anemia.
I pazienti avranno spesso bisogno di trasfusioni di sangue e oltre il 30% interromperà il trattamento a causa dell’anemia. L’anemia e la dipendenza da trasfusioni sono fortemente correlate con prognosi infausta, ridotta qualità della vita e riduzione della sopravvivenza.

